ကာဗွန်ဒိုင်အောက်ဆိုက်
ကာဗွန်ဒိုင်အောက်ဆိုဒ် (Carbon dioxide ဓာတုသင်္ကေတ CO2) သည် လေထုထဲတွင် အတွေ့များသည့် ဒြပ်ပေါင်းတစ်မျိုး ဖြစ်ပြီး အောက်စီဂျင် အက်တမ်နှစ်ခုနှင့် ကာဗွန် အက်တမ်တစ်ခု ပေါင်းစပ်ဖွဲ့စည်းထားသည်။ သာမန် လေဖိအားနှင့် အပူချိန်တွင် CO2 သည် အငွေ့အခြေအနေတွင် ရှိပြီး လေထုထဲတွင် ၀.၀၃၈ % ပါဝင်သည်။

အပင်များသည် နေရောင်ခြည်ဖြင့် အစာချက်လုပ်ရာတွင် ကာဗွန်ဒိုင်အောက်ဆိုဒ်ကို ကုန်ကြမ်းအဖြစ် သုံးသည်။ အပိုပစ္စည်းအဖြစ် သတ္တဝါများ အသက်ရှူရာတွင် လိုအပ်သည့် အောက်စီဂျင်ဓာတ်ငွေ့ကို ထုတ်လွှတ်သည်။ အရာဝတ္ထုများ မီးလောင်ကျွမ်းသည့်အခါ သို့မဟုတ် လူအပါအဝင် သတ္တဝါများ အသက်ရှူသည့်အခါ CO2 ဓာတ်ငွေ့ကို ထုတ်လွှတ်သည်။
ကာဗွန်ဒိုင်အောက်ဆိုဒ် ဓာတ်ငွေ့များသည် အပူစွမ်းအင်ကို ဖြစ်ပေါ်စေသည့် အနီအောက်ရောင်ခြည်ကို စုပ်ယူနိုင်စွမ်းရှိသောကြောင့် သိပ္ပံပညာရှင်များက CO2 အား ဖန်လုံအိမ်ဓာတ်ငွေ့ အဖြစ် သတ်မှတ်ထားသည်။ လေထုအတွင်း CO2 သိပ်သည်းဆ တိုးမြင့်လာခြင်းသည် ကမ္ဘာကြီး ပူနွေးလာစေသည့် အကြောင်းအရင်း တစ်ရပ်ဟု ပညာရှင်များက ယူဆထားကြသည်။
လေထုအတွင်း CO2 သိပ်သည်းဆများလွန်းလျှင် ဥပါဒ်ဖြစ်စေနိုင်သည်။ ၁ % အထက် ရှိလျှင် လူအချို့အား မူးဝေစေသည်။ သိပ်သည်းဆ ၇ % မှ ၁၀ % အကြား ရှိလျှင် ခေါင်းကိုက်ခြင်း၊ အကြားနှင့် အမြင်အာရုံကို ထိခိုက်စေပြီး မိနစ်ပိုင်း အနည်းငယ်မှ တစ်နာရီအတွင်း မေ့မျောသွားစေနိုင်သည်။[1]
ရုပ်ကြွင်းလောင်စာများမှ ကမ္ဘာကြီးပူနွေးပြီး ရာသီဥတု ပြောင်းလဲမှုကို ဖြစ်ပေါ်စေသည့် ကာဗွန်ဒိုင်အောက်ဆိုဒ် ဓာတ်ငွေ့ကို စွမ်းအင်ကဏ္ဍပြီးနောက် ပို့ဆောင်ရေးကဏ္ဍမှ ဒုတိယအများဆုံး ထုတ်လွှတ်လျက်ရှိကြောင်း အပြည်ပြည်ဆိုင်ရာ စွမ်းအင်အေဂျင်စီ(International Energy Agency)၏ ထုတ်ပြန်ချက်အရ သိရှိရသည်။
ကာဗွန်ဒိုင်အောက်ဆိုက်
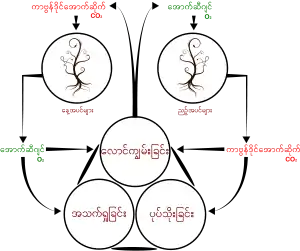
ကာဗွန်ဒိုင်အောက်ဆိုက် (ဓာတ်ငွေ့)သည် ကာဗွန်အက်တမ်တခုနှင့် အောက်ဆီဂျင် အက်တမ် နှစ်ခုတို့ ပေါင်းစပ်ဖွဲ့စည်း၍ ရရှိသောဓာတ်ငွေ့ ဖြစ်၏။ ဓါတုသင်္ကေတမှာ CO2 ဖြစ်၏။ ထိုဓာတ်ငွေ့သည် လေထု၏အပုံ တစ်သောင်းတွင် လေးပုံမျှ ပါဝင်လျက် ရှိ၏။ အရွက်စိမ်းလန်းသော အပင် များသည် အစာအာဟာရ အဖြစ်ဖြင့် ကာဗွန်ဒိုင်အောက်ဆိုဒ်(ဓာတ်ငွေ့)ကို ရှုသွင်း၍ အောက်ဆီဂျင် (ဓာတ်ငွေ့)ကို ရှုထုတ်ကြ၏။ လူနှင့်တိရစ္ဆာန်တို့ကမူ အောက်ဆီဂျင် (ဓာတ်ငွေ့)ကို ရူသွင်း၍ ကာဗွန်ဒိုင် အောက်ဆိုက်(ဓာတ်ငွေ့)ကို ရူထုတ်ကြ၏။ ဤနည်းဖြင့် သက်ရှိသတ္တဝါများက ရူထုတ်လိုက်သော ကာဗွန်ဒိုင် အောက်ဆိုက်(ဓာတ်ငွေ့)ကို အရွက်စိမ်းလန်းသော အပင်များက အစာအာဟာရအဖြစ် ရူသွင်းကြ၍၊ ထိုအပင်များမှ ရူထုတ်လိုက်သော အောက်စီဂျင်(ဓာတ်ငွေ့)ကို တဖန် သက်ရှိ သတ္တဝါများက အာဟာရအဖြစ် ရူသွင်းကြပြန်၏။ ထို့ကြောင့် လေထု၏အပုံတစ်သောင်းတွင် လေးပုံမျှ ပါဝင်သော ကာဗွန်ဒိုင်အောက်ဆိုက်၏ အချိုးသည် မည်သည့်အခါမျှ မပြောင်းလဲဘဲ တည်မြဲလျက်ရှိသည်။
ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့)သည် လေထက် တဆခွဲမျှပို၍ လေးသောကြောင့်ဂူများ၊ တောင်ကြားများ၊ မီးတောင်များ၏ အောက်မြေပြင်တလျှောက်တို့တွင်သာ ရှိတတ်၏။ ရေကဲ့သို့ တစ်နေရာမှ တစ်နေရာသို့ ခွက်များဖြင့်ထည့်၍ ယူသွားနိုင်ပြီးလျှင် သွန်ချနိုင်၏။ ထိုဓာတ်ငွေ့သည် အရောင်ကင်း၍ အနံ့လည်း မရှိ။ သို့သော် ရေတွင်ပျော်ဝင်၍ ထိုဖျော်ရည်ကို ကာဗွန်နစ်အက်ဆစ်ဟုခေါ်၏။ ထိုဖျော်ရည်ကို ဆိုဒါ၊ လင်မနစ်စသော ဘိလတ်ရည်များ ပြုလုပ်ရာ၌ များစွာ အသုံးပြုကြသည်။ ကာဗွန်ဒိုင်အောက်ဆိုက် (ဓာတ်ငွေ့)ကို ထုံးရည်ကြည်ထဲသို့ ထည့်၍လှုပ်လိုက်လျှင် နို့ရည်ကဲ့သို့ ဖြူသွား၏။ ထိုဓာတ်ငွေ့သည် ရေမှာထက် အယ်လကိုဟောတွင် ပို၍ ပျော်ဝင်လွယ်သည်။ ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့)သည် အောက်ဆီဂျင်(ဓာတ်ငွေ့)နှင့် အနည်းငယ်မျှ မတူချေ။ မီးလောင် ကျွမ်းခြင်းကို အားမပေးသည့်ပြင် မီးကို ငြိမ်းစေသည်။
ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့)ရှိသော အဝကျယ်ကျယ် ပုလင်းထဲသို့ မီးထွန်းထားသော ဖယောင်းတိုင်ကို ထည့်လိုက်လျှင် မီးငြိမ်းသွားသည်ကို တွေ့နိုင်သည်။ ထို့ကြောင့် အချို့ သော မီးသတ်ဆေးဗူးများတွင် ရုတ်တရက်မီးဘေးကိစ္စ ပေါ်ပေါက်၍ အသုံးပြုသောအခါ ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့) များကို ထုတ်ပေးနိုင်စေရန် ဓာတ်ဆေးရည်တစ်မျိုးကို ထည့်ထားတတ်၏။ တိုက်ရိုက်အားဖြင့်အဆိပ်ရှိသည်ဟု မဆိုသာသော်လည်း ကာဗွန်ဒိုင် အောက်ဆိုက် (ဓာတ်ငွေ့)စစ်စစ် ကိုဖြစ်စေ၊ ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့)-အမြောက်အမြား ပါရှိသောလေကိုဖြစ်စေ၊ ရှူမိလျှင်အောက်ဆီဂျင် လုံလောက်အောင် မရနိုင်သောကြောင့် မွန်း၍ သေဆုံးတတ်သည်။ ကာဗွန်ဒိုင်အောက်ဆိုက်(ဓာတ်ငွေ့)ကို ဖေါ်ယူသောနည်းမှာ ကယ်လဆီယမ် ကာဗွန်နိတ်ဖြစ်သော စကျင်ကျောက် သို့မဟုတ် ထုံးကျောက်ထဲသို့ ဟိုက်ဒရိုကလောရစ်အက်ဆစ် အပေါ့ရည် လောင်းထည့်သောနည်း ဖြစ်၏။ ဥဒါဟရုဏ်
| CaCo3 | + | 2HCL | = | CACL2 | + | H2O | + | CO2 |
|---|---|---|---|---|---|---|---|---|
| စကျင်ကျောက် | + | အက်စစ် | = | ဓာတ်ဆား | + | ရေ | + | ကာဗွန်ဒိုင်အောက်ဆိုက် (ဓာတ်ငွေ့) |
ရောင်းဝယ်ဖောက်ကားရန် အတွက်မူ မက်ကနီဇီယမ်ကာဗွန် နိတ်နှင့် ဆိုဒီယမ်ကာဗွန်နိတ်တို့တွင် ဆာလဖျူရစ် အက်ဆစ်ထည့်၍ ကာဗွန်ဒိုင်အောက်ဆိုက်ကို အကြီးအကျယ် ဖေါ်ယူ ထုတ်လုပ်ကြသည်။ [2]
ကိုးကား
- "Carbon Dioxide as a Fire Suppressant: Examining the Risks"၊ U.S. Environmental Protection Agency:။
- မြန်မာ့စွယ်စုံကျမ်း၊ အတွဲ(၁)