စိန်ဖြူ
စိန်ဖြူ (စိန်သတ္တုဟူ၍ မြန်မာ့စွယ်စုံကျမ်းအတွဲ-၄တွင် အဓိပ္ပါယ်ဖွင့်ဆိုထားသည်။)[7]အား အင်္ဂလိပ်ဘာသာဖြင့် အာဆင်းနစ်(Arsenic) ဟု ခေါ်ဆိုကြသည်။ ဓာတုဗေဒသင်္ကေတမှာ As ဖြစ်သည်။ အဝါ၊ အနက်၊ မီးခိုးဟူသော သုံးမျိုးစပ်အရောင်ဖြစ်ပြီး ငွေရောင်သမ်းနေသော ကြွပ်ဆတ်သည့် ပုံဆောင်ခဲအနေဖြင့် တွေ့ရပါသည်။ သံမဏိရောင် ခပ်မွဲမွဲရှိ၍ သတ္တုကဲ့သို့ပြောင် လက်သော အခဲဖြစ်၏။ ခနောက်စိမ်းနှင့် ကြွပ်တို့ကဲ့သို့ပင် သတ္တုဟုလည်း မဆိုနိုင်၊ သတ္တုမဟုတ်ဟူ၍လည်း မဆိုနိုင်သော ကြားသတ္တုဒြဗ်စင်ဖြစ်၏။ သို့သော် သတ္တုမဟုတ်သော ဖော့စဖောရစ်နှင့် ပို၍နီးစပ်၏။ အာဆင်းနစ်ကို သယံဇာတအဖြစ်ဖြင့် ၎င်း၊ အထူးသဖြင့် ကန့်နှင့် ရောစပ်၍ တွေ့နေကျသတ္တုရိုင်းများ တွင်၎င်း တွေ့ရ၏။ အခြား ဒြပ်စင်များနှင့်လည်း အလွယ်တကူ ဓာတ်ပြုနိုင်ပါသည်။ အပူပေးသောအခါ အလွယ်တကူ ကြက်သွန်နံ့ရသော အာဆင်းနစ် ထွိုင်အောက်ဆိုဒ်(arsenic trioxide) အဖြစ်သို့ ပြောင်းလဲသွားပါသည်။ non metallic form ဓာတ်ပြုအား အလွန် နည်းသော်လည်း ပြင်းအားကောင်းသည့် အက်ဆစ်များ ထဲတွင် ပျော်ဝင်နိုင်ပါသည်။
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ယေဘုယျ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| အမည်၊ သင်္ကေတ | အာဆင်းနစ်, As | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အသံထွက် | /ˈɑːrsɪnɪk/, also /ɑːrˈsɛnɪk/ when attributive AR-sə-nik, ar-SEN-ik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အော်လိုထရိုဖီ | grey (most common), yellow, black | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အဆင်း | metallic grey | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယားရှိ အာဆင်းနစ် | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တမ် အမှတ်စဉ် (Z) | 33 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အုပ်စု၊ ဘလော့ | group 15 (pnictogens), p-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယား | period 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင် ကဏ္ဍ | metalloid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| စံ အက်တောမစ် အလေးချိန် (±) (Ar) | 74.921595(6)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ပြုပြင်မှု | [Ar] 3d10 4s2 4p3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အခွံတစ်ခုလျင် အီလက်ထရွန်ပါဝင်မှု | 2, 8, 18, 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရုပ်ပိုင်းဆိုင်ရာ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖေ့စ် | အစိုင်အခဲ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sublimation point | 887 K (615 °C, 1137 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သိပ်သည်းမှု (အခန်းအပူချိန်) | 5.727 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5.22 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သုံးပွင့်ဆိုင်မှတ် | 1090 K, 3628 kPa[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Critical point | 1673 K, ? MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖျူးရှင်းအပူ | grey: 24.44 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အငွေ့ပျံခြင်း အပူ | 34.76 kJ/mol (?) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| မိုလာ အပူအင်အား | 24.64 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ငွေ့ရည်ဖိအား
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် ဂုဏ်အင်များ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အောက်ဆိုဒ်ဒေးရှင်း အခြေနေ | 5, 4, 3, 2, 1,[3] −1, −2, −3 (a mildly acidic oxide) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ဆန့်ကျင်ဘက်ဓာတ် | Pauling scale: 2.18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အိုင်ယွန်းပြုခြင်းစွမ်းအင် | 1st: 947.0 kJ/mol 2nd: 1798 kJ/mol 3rd: 2735 kJ/mol (more) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် အချင်းဝက် | empirical: 119 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ကိုဗေးလန့်အချင်းဝက် | 119±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဗန်ဒါဝေါ့စ် အချင်းဝက် | 185 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellanea | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပုံဆောင်ခဲ ဖွဲ့စည်းပုံ | rhombohedral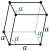 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူ ပြန့်ကားမှု | 5.6 µm/(m·K)[4] (at r.t.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူစီးကူးမှု | 50.2 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| လျှပ်စစ် ခုခံမှု | 333 nΩ·m (at 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက်ဓာတ် | diamagnetic[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက် ထိတွေ့နိုင်မှု (χmol) | −5.5·10−6 cm3/mol[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 8 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 22 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 3.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 1440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-38-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သမိုင်းကြောင်း | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရှာဖွေတွေ့ရှိမှု | အစောပိုင်း ကြေးခေတ် (ဘီစီ ၂၅၀၀) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပထမဆုံး ခွဲထုတ်မှု | Albertus Magnus (1250) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Most stable isotopes of အာဆင်းနစ် | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
အသုံးပြုခြင်း
အခြားဓာတ်ပေါင်းများနှင့် ရောစပ်ထားသော အာဆင်းနစ်သည် အာစနစ်ချည်းသက်သက်ထက်ပို၍ အသုံးဝင်သည်။ အာဆင်းနစ် ဒြပ်ပေါင်းများကို ဖန်ထည်များ ပြုလုပ်ခြင်း၊ လေဆာရောင်ခြည် ထုတ်လွှတ်နိုင်သော semiconductor gallium arsenade ပြုလုပ်ခြင်းတို့တွင် အသုံးပြုပါသည်။ Arsine gas AsH3 သည် လွန်စွာ အဆိပ်ပြင်းသောကြောင့် အထူးဂရုပြု သုံးရသော်လည်း ၎င်းကို အီလက်ထရွန်းနစ် ပစ္စည်းပြုလုပ်သော စက်ရုံများတွင် အဓိက အရေးကြီးဓာတ်ငွေ့အဖြစ် အသုံးပြုကြပါသည်။ အာဆင်းနစ်ဒြဗ်ပေါင်းများ သည် အမျိုးမျိုးသော အသီးပင် အရွက်ပင်များကို ဖျက်ဆီးတတ်သော ပိုးမွှားများကို သတ်ရန် ပိုးသတ်ဆေး အဖြစ်ဖြင့် အလွန်အသုံးဝင်၏။ ကော့ပါး(ကြေးနီ)၊ ဟိုက်ဒရိုဂျင်၊ အောက်စီဂျင်တို့နှင့် ရောစပ် ထားသော အာစနစ်ဒြဗ်ပေါင်းများကို ခြယ်ဆေးပေါင်း မြောက်များစွာတို့တွင် အသုံးပြုရ၏။ အနုပညာတွင် အသုံးများသော မြစိမ်းရောင်အသွေး ရှိသည့် 'ပဲရစ် ဂရင်း(copper acetoarsenite)'ခေါ် ထင်ရှားသော ခြယ်ဆေးတစ်မျိုးတွင် အာစနစ်ပါ၏။ အာဆင်းနစ် ဒြဗ်ပေါင်းများမှ အဆိပ်ငွေ့များ ထွက်မည်ဟု ယူဆကြသဖြင့် နံရံကပ်စက္ကူများနှင့်အထည် များကို အာဆင်းနစ်ပါသော ဆိုးဆေးများဖြင့် အရောင်ခြယ်လေ့ ဆိုးလေ့မရှိကြချေ။
အာဆင်းနစ်ကို ခဲကျည်ဆန်များပြုလုပ်ရာတွင် အဓိကအသုံး ပြုကြ၏။ ကျည်စေ့များပြုလုပ်ရာ၌ ခဲတွင် အာဆင်းနစ် အနည်းငယ်ကိုထည့်၍ ရောစပ်အသုံးပြုခြင်းဖြင့် ကျည်စေ့လုံးကလေး များကို ရရှိနိုင်သည်။ ခဲချည်း သက်သက်ကို ကျို၍လောင်းယူလျှင် အလုံးကလေးများကို မရနိုင်ဘဲ၊ အမျှင်တန်းလန်းပါလာသော ခဲကလေးများကိုသာရရှိသည်။ အာဆင်းနစ်နှင့် အောက်စီဂျင် ရောစပ်ထားသော အာဆင်းနစ်အဖြူကို ဖန်လုပ်ငန်းတွင် သံကြောင့်ဖြစ်ပေါ်သော အရောင်ကိုချွတ်ရန် အသုံးများ၏။ ထို့ပြင် ကြွက်နှင့်ယင်များကိုသတ်ရန် အဆိပ်ခတ်ဆေးအဖြစ်ဖြင့်၎င်း၊ ရောင်စုံ မီးပန်းများ ပြုလုပ်ရာ၌၎င်း အသုံးပြုကြသေး၏။ အိုင်းယန်းပါကလိုရိုက် ပျော်ဝင်ရည်နှင့် မက်ဂနီဇီယာအမှုန့်များသည် အာဆင်းနစ်အဆိပ်ဖြေဆေးများဖြစ်ကြသည်။ သံတွင် အာဆင်းနစ် အနည်းငယ်ထည့်၍ ရောစပ်လိုက်သောအခါ သံအရောင်ပြောင်လက်၍လာသည်။
သဘာဝမှာတွေ့ရှိရမှုအခြေအနေ
အာဆင်းနစ်သည် သဘာဝတွင် အနည်းငယ်သာတွေ့ရပါသည်။ ၎င်းသည် မြေဆီလွှာထဲတွင် ဖြစ်ပေါ်ပြီး လေနှင့် ရေတို့မှတစ်ဆင့် နေရာအနှံ့အပြားသို့ပျံ့နှံ့ သွားပါသည်။ အာဆင်းနစ်သည် သေစေနိုင်သော အဆိပ်ရှိသော်လည်း တချို့သက်ရှိများအတွက် အနည်းငယ် လိုအပ်ပါသည်။ သန့်စင်သော အာဆင်းနစ် ကို သဘာဝတွင် microcrystalline အဖြစ်နှင့်သာ အနည်းအပါး တွေ့ရပါသည်။ ၎င်းကို ဆိုက်ဘေးရီးယား၊ ဂျာမနီ၊ ပြင်သစ်၊ အီတလီ၊ ရိုမေးနီးယားနှင့် အမေရိကန်နိုင်ငံ တို့တွင်တွေ့ရပါသည်။ အာဆင်းနစ်ကို အများအားဖြင့် ဆာလ်ဖာနှင့် ရောစပ်ပြီး arsenopyrite (AsFeS) တွင်တွေ့ရပါသည်။[8] [9]
 အကြီးဆုံးနှင့် အခြေခံကျဆုံး သဘာဝ စိန်ဖြူတုံးကြီး
အကြီးဆုံးနှင့် အခြေခံကျဆုံး သဘာဝ စိန်ဖြူတုံးကြီး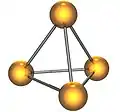 အဝါရောင် စိန်ဖြူAs4 နှင့် အဖြူရောင် ဖော့စဖောရပ်P4တို့၏ ပုံစံ
အဝါရောင် စိန်ဖြူAs4 နှင့် အဖြူရောင် ဖော့စဖောရပ်P4တို့၏ ပုံစံ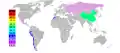 ကမ္ဘာ့ စိန်ဖြူထွက်ရှိမှုနှုံးပြ မြေပုံ
ကမ္ဘာ့ စိန်ဖြူထွက်ရှိမှုနှုံးပြ မြေပုံ သဘာဝအခြေအနေ
သဘာဝအခြေအနေ
ကိုးကား
- Standard Atomic Weights 2013. Commission on Isotopic Abundances and Atomic Weights
- Gokcen, N. A (1989). "The As (arsenic) system". Bull. Alloy Phase Diagrams 10: 11–22. doi:.
- "Stabilized Arsenic(I) Iodide: A Ready Source of Arsenic Iodide Fragments and a Useful Reagent for the Generation of Clusters" (2004). Inorganic Chemistry 43 (19): 5981–6. doi:. PMID 15360247.
- Cverna, Fran (2002)။ ASM Ready Reference: Thermal properties of metals။ ASM International။ pp. 8–။ ISBN 978-0-87170-768-0။ pdf.
- Lide, David R., ed. (2000)။ "Magnetic susceptibility of the elements and inorganic compounds"။ Handbook of Chemistry and Physics (PDF) (81 ed.)။ CRC press။ ISBN 0849304814။
- Weast၊ Robert (1984)။ CRC, Handbook of Chemistry and Physics။ Boca Raton, Florida: Chemical Rubber Company Publishing။ pp. E110။ ISBN 0-8493-0464-4။
- မြန်မာ့စွယ်စုံကျမ်း၊ အတွဲ(၄)
- ဒြပ်စင်အလှည့်ကျဇယားဘာသာပြန်ဆိုမှု ပရောဂျက်တွင် ပါဝင်သူ ကိုတင်ကျော်ဦးမှ ဘာသာပြန်ဆိုသည်။
- မြန်မာ့စွယ်စုံကျမ်း၊ အတွဲ(၄)
| ဝစ်ရှင်နရီ၊ အခမဲ့အဘိဓာန်တွင် စိန်ဖြူ ကို ရှာဖွေကြည့်ရှုပါ။ |
