သံဖြူ
သံဖြူ (ခဲမဖြူ) သည် ပျော့ပျောင်း၍ အလွယ်တကူပုံသွင်းနိုင်သော ငွေဖြူရောင် သတ္တု တစ်မျိုးဖြစ်သည်။ အောက်ဆီဂျင်နှင့် အလွယ်တကူ ဓာတ်ပြုခြင်း မရှိသောကြောင့် သံချေးတက်ခြင်းမှ ကာကွယ်ပေးနိုင်သည်။ တင်း(Tin)သည်ပင်လယ်ရေနှင့် သိုလှောင်ထားသော ရေများကြောင့် အလွယ်တကူသံချေးမတက်နိုင်ပေ။ သံဖြူသည် ဓာတု ဒြပ်စင်တစ်ခုဖြစ်ပြီး အက်တမ်အမှတ်စဉ်မှာ ၅၀ဖြစ်ကာ ယင်း၏ ဓာတုဗေဒ သင်္ကေတမှာ Sn ဖြစ်သည်။ ၎င်းကို တင်းဒိုင်အောက်ဆိုဒ်, SnO2 ပါဝင်သည့် တွင်းထွက်ပစ္စည်း ကက်စီတာရိုက်မှ အဓိကရရှိသည်။ သံဖြူသည် နံပတ် ၄၉ မြောက် အများဆုံး တွေ့ရသည့် ဒြပ်စင်ဖြစ်ပြီး ယင်း၏ ထူးခြားသည့် ပရိုတွန်အရေအတွက်ကြောင့် ဒြပ်စင်အလှည့်ကျဇယားတွင် တည်ငြိမ်သည့် အိုင်ဆိုတုပ် အများဆုံးဖြစ်သည့် ၁၀ မျိုးရှိသည်။
 left: white, beta, β; right: gray, alpha, α | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ယေဘုယျ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| အမည်၊ သင်္ကေတ | သံဖြူ, Sn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အသံထွက် | /ˈtɪn/ TIN | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အော်လိုထရိုဖီ | alpha, α (gray); beta, β (white) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အဆင်း | silvery-white (beta, β) or gray (alpha, α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယားရှိ သံဖြူ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တမ် အမှတ်စဉ် (Z) | 50 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အုပ်စု၊ ဘလော့ | group 14 (carbon group), p-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယား | period 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင် ကဏ္ဍ | post-transition metal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| စံ အက်တောမစ် အလေးချိန် (±) (Ar) | 118.710(7)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ပြုပြင်မှု | [Kr] 4d10 5s2 5p2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အခွံတစ်ခုလျင် အီလက်ထရွန်ပါဝင်မှု | 2, 8, 18, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရုပ်ပိုင်းဆိုင်ရာ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖေ့စ် | အစိုင်အခဲ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အရည်ပျော်မှတ် | 505.08 K (231.93 °C, 449.47 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အရည်ဆူမှတ် | 2875 K (2602 °C, 4716 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သိပ်သည်းမှု (အခန်းအပူချိန်) | white, β: 7.265 g/cm3 gray, α: 5.769 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6.99 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖျူးရှင်းအပူ | white, β: 7.03 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အငွေ့ပျံခြင်း အပူ | white, β: 296.1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| မိုလာ အပူအင်အား | white, β: 27.112 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ငွေ့ရည်ဖိအား
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် ဂုဏ်အင်များ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အောက်ဆိုဒ်ဒေးရှင်း အခြေနေ | 4, 3,[2] 2, 1,[3] −1, −2, −3, −4 (an amphoteric oxide) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ဆန့်ကျင်ဘက်ဓာတ် | Pauling scale: 1.96 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အိုင်ယွန်းပြုခြင်းစွမ်းအင် | 1st: 708.6 kJ/mol 2nd: 1411.8 kJ/mol 3rd: 2943.0 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် အချင်းဝက် | empirical: 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ကိုဗေးလန့်အချင်းဝက် | 139±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဗန်ဒါဝေါ့စ် အချင်းဝက် | 217 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellanea | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပုံဆောင်ခဲ ဖွဲ့စည်းပုံ | tetragonal white (β) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပုံဆောင်ခဲ ဖွဲ့စည်းပုံ | face-centered diamond-cubic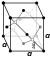 gray (α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အသံ၏အမြန်နှုန်း ပါးလွှာသော သံချောင်း | 2730 m/s (at r.t.) (rolled) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူ ပြန့်ကားမှု | 22.0 µm/(m·K) (at 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူစီးကူးမှု | 66.8 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| လျှပ်စစ် ခုခံမှု | 115 nΩ·m (at 0 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက်ဓာတ် | gray: diamagnetic[4] white (β): paramagnetic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက် ထိတွေ့နိုင်မှု (χmol) | (white) +3.1·10−6 cm3/mol (298 K)[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 50 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 18 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 58 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပိုင်ဆွန် အချိုး | 0.36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 50–440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-31-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သမိုင်းကြောင်း | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရှာဖွေတွေ့ရှိမှု | ခရစ်မပေါ်မီ ၃၅၀၀ ဝန်းကျင် | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Most stable isotopes of သံဖြူ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ဘီစီ ၃၀၀၀ ခန့်ကတည်းက လူသားတို့ ပထမဆုံး သတ္တုစပ်အဖြစ် အမြောက်အများ အသုံးပြုခဲ့သည့် အရာမှာ ကြေးနီနှင့် သံဖြူကို ရောစပ်ထားသည့် ကြေးညိုဖြစ်သည်။ ဘီစီ ၆၀၀ နောက်ပိုင်းတွင် သံဖြူ သတ္တုစင်ကို ထုတ်လုပ်နိုင်ခဲ့ကြသည်။ ကြေးခေတ်မှ ၂၀ရာစုအထိ သံဖြူ ၈၅- ၉၀%နှင့် အကျန်ကို ကြေး၊ ခဲနှင့်အန်တီမိုနီတို့ကို ပေါင်းစပ်ထားသည့် လောဟာ/ဘင်သတ္တုစပ်ကို ပန်းကန်ပြား၊ လင်ပန်းစသည်တို့အဖြစ် အသုံးပြုခဲ့ကြသည်။ ယနေ့ခေတ်တွင် သံဖြူကို သတ္တုစပ်အဖြစ် အသုံးများကြပြီး သံဖြူ ၆၀%ကျော် ပါဝင်သည့် သံဖြူ/ခဲစပ် ခဲဂရေဆော်ရာတွင် အများဆုံးအသုံးပြုသည်။ သံဖြူအား နောက်ထပ်အများအပြား အသုံးပြုမှုတစ်ခုမှာ သံမဏိကို သံချေးတက်မှုမှ ခံနိုင်ရည်ရှိအောင် သံဖြူရည်စိမ်ခြင်းဖြစ်သည်။ ယင်း၏အဆိပ်ဖြစ်မှုနည်းပါးမှုကြောင့် သံဖြူစိမ်သတ္တု (သံမဏိ/ဒန်)တို့ကို အစားအသောက်များထည့်သည့် စည်သွပ်ဘူးများအဖြစ်လည်း အသုံးပြုကြသည်။
အသုံးပြုခြင်း
တင်း(Tin) ကို coating ပြုလုပ်ရာတွင် အသုံးပြုပြီး၊ အထူးသဖြင့် အစားအစာ စည်သွတ်ဘူးပြုလုပ်ရာတွင် Tin coating လုပ်ထားသော သံဗူးများကို အများဆုံးအသုံးပြုသည်။ Tin ပါဝင်သော သတ္တုစပ် (alloys) များကို ပိုက်ဆက်ခြင်း၊ လျှပ်စစ် circuits များချိတ်ဆက်ခြင်း၊ pewter, bell metal, babbit metal နှင့် dental amalgams စသည်တို့ ပြုလုပ်ရာတွင် အသုံးပြုသည်။ niobium-tin သတ္တုစပ်ကို superconduction magnets တွင်လည်းကောင်း၊ tin oxide ကို ကြွေထည်မြေထည် နှင့် gas sensors or gas detector များတွင် အသုံးပြုသည်။ Tin သတ္တုပြားများကို ယခင်က အစားအသောက်များ၊ ဆေးဝါးများ ထုပ်ပိုးရာတွင် အသုံးပြုသော်လည်း ယခုအခါ aluminium သတ္တုပြားများ ပိုမို အသုံးပြုလာသည်။
သဘာဝတွင် တွေ့ရှိမှု အခြေအနေ
Tin oxide သည်ပျော်ဝင်မှုမရှိပဲ ရာသီဥတုဒဏ်ခံနိုင်သဖြင့် မြေထုနှင့် သဘာဝရေထဲတွင် ပါဝင်မှုနည်းသည်။ တချို့မြေကြီးတွင် 1-4 ppm ခန့်ပါဝင်ပြီး၊ တချို့ မြေတွင်မူ 0.1 ppm ထက်လျော့နည်းသည်။ မြေကြီးတွင် Tin oxide အများဆုံးပါဝင်နိုင်မှုမှာ 300 ppm ခန့်ဖြစ်သည်။ သဘာဝအသီးအရွက်နှင့် စားသုံးနေသော အသားများတွင် tin ပါဝင်မှုအနည်းငယ်ရှိသည်။ တင်းသတ္တုအလွှာ(tin belt) ထုတ်ယူနိုင်သော သတ္တုထုတ်လုပ်ရာနေရာ (mining area) ကို တရုတ်ပြည်မှ စတင်ပြီး ထိုင်း၊မြန်မာ၊မလေးရှားတို့ကိုဖြတ်ပြီး အင်ဒိုးနီးရှား ကျွန်းဆွယ်အထိ ရှည်လျားစွာ တွေ့ရသည်။ မလေးရှားသည် ကမ္ဘာပေါ်တွင် တင်း(Tin) ထုတ်လုပ်မှု၏ 40% ကို ရှိသည်။ Bolivia နှင့် Brazil တို့တွင်လည်း Tin mine များကိုတွေ့ရသည်။ ကမ္ဘာပေါ်တွင် တစ်နှစ်လျှင် တင်း(Tin) ၁၄၀ တန် ထုတ်လုပ်လျက်ရှိပြီး ထုတ်လုပ်နိုင်မှု 4 million tones အထိရှိသည်။ တင်း(Tin)ပါဝင်သောပစ္စည်းများတွင် လောလောဆယ် အသုံးပြုမှုမှာ တစ်နှစ်လျှင် ၁၃၀ တန်ခန့်ဖြစ်သည်။
ကျန်းမာရေးအပေါ် သက်ရောက်မှုများ
တင်း(Tin) သည်အဓိကအားဖြင့် အမျိုးမျိုးသော organic substances များနှင့် တွဲစပ်နိုင်သည်။ ထို organic tin bonds များသည် လူအတွက် အန္တရာယ် အများဆုံးဖြစ်သည်။ organic tin bonds များကို စက်ရုံများတွင် အများအပြား တွေ့ရတတ်သည်။ ဥပမာ- ဆေး(သုတ်ဆေး)စက်ရုံ၊ ပလပ်စတစ် စက်ရုံ၊ စိုက်ပျိုးရေးနှင့် ဆိုင်သော ပိုးမွှားသတ် ပစ္စည်းထုတ်လုပ်မှုလုပ်ငန်းများ။ organic tin substances တွေဟာတိုးပွားလျှက်ရှိပြီး လူတွေအတွက် အဆိပ်အတောက် တစ်ခုသဖွယ်လက်ခံထားကြသည်။ ၎င်းတို့၏ သက်ရောက်မှုသည် organic ထဲတွင် ပါဝင်သော substance အမျိုးအစားပေါ်မူတည်၍ အမျိုးမျိုးကွဲပြားသည်။ ထိုထဲမှ Triethyltin သည် လူတို့အတွက် အန္တရာယ်အများဆုံး organic tin substance တစ်ခုဖြစ်တယ်။ ၎င်းထဲတွင် hydrogen bonds ပါဝင်မှုရှိပြီး၊ hydrogen bonds ပါဝင်မှုကြီးလေလေ tin substance ရဲ့အန္တရာယ်လျှော့ နည်းလေလေဖြစ်သည်။ လူသည် tin bonds များကို အစားအစာများမှလည်းကောင်း၊ အရေပြားကိုဖြတ်၍လည်းကောင်း စုပ်ယူနိုင်တယ်။ tin bonds များကို အသက်ရှူသွင်းခြင်းဖြင့် ရေရှည်တွင် ဆိုးကျိုးများ ဖြစ်စေနိုင်သည်။
အဓိကဖြစ်စေနိုင်သော သက်ရောက်မှုများမှာ –
- မျက်စိနှင့် အသားအရေကို ထိခိုက်နိုင်သည်
- ခေါင်းမူး၊ ခေါင်းကိုက် ဖြစ်စေနိုင်သည်
- အစာအိမ် ထိခိုက်နိုင်သည်
- ဖျားနာခြင်း၊ အတွေးအခေါ်ရှုပ်ထွေးခြင်းများ ဖြစ်စေနိုင်သည်
- ပြင်းထန်သော စိတ်ဖိစီးမှု ခံစားရခြင်း၊ အသက်ရှူမဝခြင်းတို ့ ဖြစ်စေနိုင်သည်
- ဆီးနှင့် ပက်သက်သော ပြဿနာများ ဖြစ်စေနိုင်သည်။
ရေရှည်တွင် ဖြစ်ပေါ်နိုင်သော ဆိုးကျိုးများမှာ –
- စိတ်ဖိစီးမှုများ
- အသည်းထိခိုက်မှု
- ကိုယ်ခံအားကျဆင်းခြင်း
- ခရိုမိုဆုန်း (Chromosome)များထိခိုက်ပျက်စီးခြင်း
- သွေးနီဥများ သက်တမ်းတိုခြင်း
- စိတ်တိုလွယ်ခြင်း၊ အိပ်မပျော်ခြင်း၊ မေ့ပျောက်လွယ်ခြင်း၊ ခေါင်းမူး ခေါင်းကိုက်ခြင်း အစရှိသော ဦးနှောက်ပိုင်းဆိုင်ရာ ထိခိုက်မှုများ ဖြစ်ပေါ်နိုင်သည်။
ပတ်ဝန်းကျင်သို့ သက်ရောက်မှု အခြေအနေ
တင်း(Tin)၏ single atoms သို့မဟုတ် molecules များသည် လူတို့၏ organism ကို အဆိပ် မဖြစ်စေနိုင်ပါ။ ၎င်းပါဝင်သော organic form တွေကသာ လူတွေကို အဆိပ်အတောက် ဖြစ်စေနိုင်သည်။ Organic tin components တွေဟာ သဘာဝပတ်ဝန်းကျင်ထဲမှာ အချိန်ကြာမြင့်စွာရှိနေနိုင်ပြီး အလွယ်တကူမပြို ကွဲနိုင်ပေ။ Microrganisms ဟာ organic tin compounds တွေကိုခွဲထုတ်ပေးပြီး ရေအောက်ကြမ်းပြင်ပေါ်တွင် စုစည်းပေးနေသည်။ ထို့ကြောင့် organic tins တွေ တိုးပွါးလျက်ရှိနေသည်။ Organic tins များသည် စွန့်ပစ်ပစ္စည်းများမှ တဆင့် ရေထဲတွင် ပျံ့နှံ့လာနိုင်သည်။ ထို့ကြောင့် fungi, algae နှင့် phytoplankton အစရှိသည့် ရေနေသတ္တဝါများ၊ အပင်များကို များစွာ အဆိပ်ဖြစ်နေနိုင်သည်။ Phytoplankton သည် aquatic ecosystem တွင် အရေးပါပြီး၊ အခြား ရေအောက်ရှင်သန်မှုများအတွက် oxygen ကိုလည်း ထုတ်လုပ်ပေးသည်။ ၎င်းသည် ရေအောက်အစားအစာအတွက်လဲ အရေးပါသည်။ Tributyltins များသည် ငါးနှင့် fungi တွေကိုအဓိက အန္တရာယ်ဖြစ်စေနိုင်ပြီး၊ phytoplankton များကို ပို၍ပင် အဆိပ်ဖြစ်စေနိုင်သည်။ Organic tins များသည် ပြန်လည်ထုတ်လုပ်ခြင်း၊ အစာချေဖျတ်မှု စနစ် နှင့် ရေနေသတ္တဝါများ၏ အစားအစာ များအပေါ် ပြင်းထန်စွာ အနှောက်အယှက်ပေးလျက်ရှိသည်။ tin compounds များသည် အဓိကအားဖြင့် ရေထု၏ အပေါ်ဆုံးအလွှာတွင် အများဆုံးပါဝင်နေတတ်သည်။
သမိုင်းမတင်မီအလွန်ရှေးကျသောအခါက လူတို့သည်ကြေးနီနှင့်သံဖြူ၊ သို့မဟုတ်ခဲမ ဖြူရောစပ်ထားသော ဗရွန်း(ကြေးညို)ခေါ် သတ္တုစပ်ကိုမိမိတို့လိုရာလက်နက်အဖြစ် လုပ်ကိုင်ခဲ့သည်။
ထိုခေတ်ကတည်းကသံဖြူပေါ်ပေါက်လာခဲ့လေသည်။ သံဖြူသည်ဒြဗ်စင်တစ်ခုဖြစ်သည်။ အက်တမ်အ မှတ် မှာ ၅ဝ ဖြစ်၍ အက်တမ်အလေးဆမှာ ၁၁၈.၇ ဖြစ်သည်။ သံဖြူထွက်သည့်ဒေသများမှာ မလေးရှားပြည်ထောင်စု၊ ဗိုလစ်ဗီးယားနိုင်ငံ၊ အင်ဒိုနီးရှားနိုင်ငံ၊ တုတ်နိုင်ငံ၊ နိုင်ဂျီးရီးယားနိုင်ငံ၊ ဗြိတိန်၊ ဩစတြေးလီးယားနိုင်ငံ၊ တပ်စနေးနီးယားကျွန်း၊ တောင်အာ ရိကနိုင်ငံ၊ ယိုးဒယားနိုင်ငံစသည်တို့ဖြစ်သည်။
ကမ္ဘာတစ်ဝှမ်းလုံးမှထွက်သည့်သံဖြူအားလုံး၏ သုံးပုံတစ်ပုံ မှာမလေးရှားပြည်ထောင်စုမှထွက်သည်။ မြန်မာနိုင်ငံတွင်လည်းကယားပြည်နယ်၊ မော်ချီးမိုင်းနှင့်သထုံ၊ မော်လမြိုင်၊ ထားဝယ်၊ မြိတ်ခရိုင်များတွင်သံဖြူထွက်သည်။ သံဖြူထုတ်ယူရသောသတ္တုရိုင်းများတွင် သံဖြူကျောက် (တင်းစတုန်း)မှာ အရေးကြီးဆုံးဖြစ်၏။
သံဖြူသည်သတ္တုရိုင်းကျောက်တုံးများထဲတွင် အနှံ့အပြား ကြဲ၍ပါဝင်သောကြောင့် သတ္တုရိုင်းအားလုံးကို ပထမမှုန့်မှုန့်ညက်ညက်ကြေအောင်ချေပြီးနောက် အထပ်ထပ်ဆေးကြောတိုက်ချွတ်ကာအခြားအညစ်အကြေး များကိုထုတ်ပစ်ရသည်။
ထိုနောက်မီးဖိုထဲ၌အပူပြင်းတိုက်ပေးခြင်းဖြင့် ကျန်နေသောမသန့်ရှင်းသည့်ဝတ္တု တို့ကိုဖယ်ထုတ်သည်။ ထိုကဲ့သို့ပြုလုပ်ပြီးသောအခါတွင်သံဖြူအစစ်ကိုရရှိလေသည်။ သံဖြူအစစ်မှာအဖြူရောင်ဖြစ်၍ ရံဖန်ရံခါတွင်သာ အပြာရောင်အနည်းငယ်မျှသန်းနေသယောင် ယောင်တွေ့ရ၏။ သံဖြူသည်အတော်အတန်အရောင်တောက်၍ လေသလပ်ခံထားခြင်းဖြင့် ကြေးညှင်း တက် ခြင်းမရှိချေ။ သံဖြူသည်ပုံဆောင်ခဲများအနေဖြင့်တည်ရှိသောဝတ္တုတစ်မျိုးဖြစ် သည်။ သံဖြူချောင်းတစ်ချောင်းကိုကွေးကြည့်ပါက ပုံဆောင်ခဲများအချင်းချင်းပွတ်မိကြသည့်အသံကိုကြားနိုင်သည်။ အလွန့်အလွန်အေးသောအပူချိန်တွင် သံဖြူသည်ကြွပ်ဆတ်လွန်း ၍ အမှုန့်အဖြစ်သို့ပင် ပြောင်းလဲသွားတတ်၏။ သို့သော် သာမန်အပူချိန်များတွင် သံဖြူသည်အတော်ပင်ပျော့ပျောင်း၍အထုအရိုက်ခံသည်။ ဤသို့အထုအရိုက်ခံနိုင်ခြင်းမှာသံဖြူ၏အရေးကြီးသော ဂုဏ်တစ်ရပ်ဖြစ်သည်။
အလွန်ပါးလွှာသွားသည့်သံဖြူပြားကလေးများဖြင့်ချော့ ကလက်၊ တော်ဖီစသည်တို့ကိုရစ်ပတ်ထုပ် ထားသည်ကိုတွေ့ကြ ရပေမည်။ ထိုပြင်သွားတိုက်ဆေး၊ပန်းချီဆေးဘူးတို့ကို ဖြစ်ညှစ်နိုင်စေရန် သံဖြူနှင့် ပြုလုပ်ထားသည်ကိုလည်းတွေ့ကြ ရပေမည်။ စည်သွတ်အစားအစာတို့ထည့်ထားသည့် သံစည်ဘူးများသည် သံဖြူဖြင့်ပြုလုပ်ထားသည် ဆိုသော်လည်းသံဖြူအစစ်မဟုတ်ကြချေ။ အမှန်မှာသံဘူးများဖြစ်၏။ သို့သော် သံသည်အစားအစာ၌ ပါရှိသောအက်ဆစ်ဓာတ်နှင့်တွေ့သောအခါ အစားအစာကိုမကောင်း အောင်လုပ်တတ် သောကြောင့် သံပြားကိုသံဖြူရည်စိမ်ကာ သံဖြူဖြင့်ဖုံးအုပ်ထားခြင်းဖြစ်လေသည်။ သံဖြူသည်အစားအစာ ကိုမည်သို့မျှမထိခိုက်နိုင်ချေ။ ရှေးကသံဖြူကို ပြဒါးနှင့်ရောစပ်၍ကြည့်မှန်၏ ကျောဘက်တွင်သုတ်လိမ်းခဲ့ ကြ၏။ သံဖြူသည်စင်တီဂရိတ် ၂၃၁.၉ ဒီဂရီမျှလောက်တွင်အရည်ပျော်သောကြောင့် သံဖြူကိုခဲနှင့် ရောစပ်ကာဂဟေဆော်ရာ၌၎င်းအသုံးပြုကြလေသည်။
သံဖြူကိုသံဖြူအဖြစ်ဖြင့် အသုံးပြုနိုင်သည့်အပြင် သတ္တုစပ်အဖြစ်ဖြင့်လည်းအသုံးပြုနိုင်သည်။သံ ဖြူကိုကြေးနီ နှင့်၎င်း၊ ခဲနှင့်၎င်း၊ ခဲနှင့်အင်တီမိုနီတို့နှင့်၎င်း ရောစပ်၍သတ္တုစပ်များပြုလုပ်နိုင်ပေသည်။
သံဖြူ၏ဒြဗ်ပေါင်းများတွင်ကလိုရင်းနှင့်ပေါင်းစပ်ထား
သော တင်းတက်တြာကလိုရိုက်ဆိုသည့် အရည်ကိုပိုးထည်များ
အလေးချိန်တိုးအောင် ဆိုးဆေး၌ထည့်ရန်အတွက်၎င်း
၊စစ်မြေပြင်တွင်မီးခိုးလုံးကြီးများ ထုတ်ရန်အတွက်၎င်း၊
အသုံးပြုကြလေသည်။
ယခုအခါတွင် ဗိုလစ်ဗီးယားနိုင်ငံသံဖြူတွင်းများမှအပ အခြားအရပ်ရပ်ရှိသံဖြူတွင်းတို့မှာတစ်နေ့ ထက်တစ်နေ့ အထွက်လျော့နည်း၍လာရာ သိပ္ပံပညာရှင်ကြီးများသည် နောင်နှစ်များမကြာမီအတွင်း၌ ကမ္ဘာတစ်ဝှမ်းလုံးရှိသံဖြူအထွက် လုံးဝရပ်စဲသွားမည်ကိုပင် စိုးရိမ်နေကြလေသည်။[6]
ကိုးကား
- Standard Atomic Weights 2013. Commission on Isotopic Abundances and Atomic Weights
- SnH3။ NIST Chemistry WebBook။ National Institure of Standards and Technology။ 23 January 2013 တွင် ပြန်စစ်ပြီး။
- HSn။ NIST Chemistry WebBook။ National Institute of Standards and Technology။ 23 January 2013 တွင် ပြန်စစ်ပြီး။
- Lide, D. R., ed. (2005)။ "Magnetic susceptibility of the elements and inorganic compounds"။ CRC Handbook of Chemistry and Physics (PDF) (86th ed.)။ Boca Raton (FL): CRC Press။ ISBN 0-8493-0486-5။
- Weast၊ Robert (1984)။ CRC, Handbook of Chemistry and Physics။ Boca Raton, Florida: Chemical Rubber Company Publishing။ pp. E110။ ISBN 0-8493-0464-4။
- မြန်မာ့စွယ်စုံကျမ်း၊ အတွဲ(၁၃)